2024年,mRNA技术在全球范围内取得了众多突破性进展,从预防性疫苗到治疗性疫苗,再到罕见病治疗药物和in vivo CAR,mRNA技术的应用范围不断拓展,为人类健康带来了新的希望。本文将为您盘点2024年mRNA领域的重大事件。
一、政策与政府支持:为mRNA技术发展铺平道路
01 中国国家药品监督管理局规范mRNA疫苗研发
2024年8月,国家药品监督管理局药品评审中心公开征求《预防用mRNA疫苗非临床研究技术指导原则(征求意见稿)》的意见通知,为规范和指导mRNA疫苗的非临床研究。
02 英国NHS计划开展万人mRNA个性化肿瘤疫苗治疗项目
2024年5月,英国国民医疗服务体系(NHS)牵头启动“癌症疫苗启动平台(Cancer Vaccine Launch Pad,CVLP)”项目,该项目计划到2030年约1万名癌症患者能通过CVLP获得个性化的肿瘤疫苗治疗。
03 韩国政府大力资助mRNA疫苗项目
2024年8月,韩国科技信息通信部宣布,韩国政府将首次大力资助建立mRNA疫苗技术开发项目,总投资达2.1万亿韩元(约合113亿人民币)。韩国政府豁免了mRNA疫苗的可行性研究,加速其研发进程。
04 俄罗斯卫生部计划推出免费mRNA肿瘤疫苗
2024年12月,俄罗斯卫生部宣布开发出一种使用mRNA技术的个性化肿瘤疫苗,并计划于2025年初免费向本国患者提供,每剂疫苗的费用由政府承担。
二、mRNA 1.0的进阶 - 非新冠mRNA疫苗的商业化破冰
2024年,全球首款非新冠病毒mRNA疫苗上市,推动了mRNA技术在疫苗研发中的多元化发展。与此同时,国内mRNA疫苗的研发也呈现出蓬勃发展的态势,在预防性疫苗和肿瘤治疗疫苗领域均展现出巨大潜力。
01 全球首款mRNA RSV疫苗获批上市
2024年5月,Moderna公司宣布其RSV mRNA疫苗mRNA-1345获得FDA批准上市。该疫苗用于预防60岁及以上成人RSV相关下呼吸道疾病(RSV-LRTD)和急性呼吸疾病(ARD)。该疫苗的成功上市也标志着mRNA技术在新冠病毒疫苗之外的疾病领域成功实现商业化破冰。
02 中国mRNA预防性疫苗管线进入快车道
截至日前,国内超20个mRNA预防性疫苗申报临床,这些疫苗涵盖了呼吸道合胞病毒(RSV)、带状疱疹病毒、单纯疱疹病毒和狂犬病病毒等多种适应症。其中针对呼吸道合胞病毒(RSV)的管线尤为突出,已有13个项目在中国或美国递交了临床试验申请(IND),带状疱疹也有8个管线在中国或者美国两地申报。众多中国创新药企纷纷入局,显现了mRNA技术在预防性疫苗领域的广阔前景。
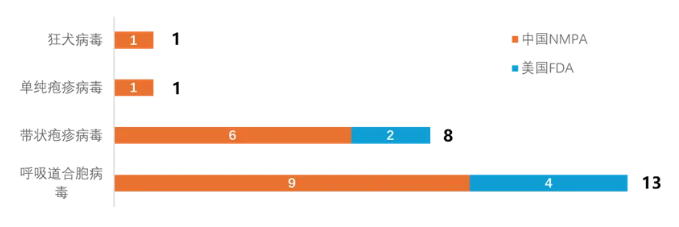
中国mRNA预防性疫苗管线在NMPA及FDA的IND申报统计
03 mRNA通用型肿瘤疫苗的多靶点国内进入临床
mRNA技术的出现让不同肿瘤疫苗成为可能,目前已经有多种不同抗原的mRNA疫苗进入管线研究,包括编码病毒抗原的基础肿瘤疫苗、编码肿瘤抗原的特异性疫苗、编码免疫调节因子的mRNA。
2024年,中国多个mRNA肿瘤疫苗管线进入临床申报阶段,涵盖了HPV、EBV、肝癌、胃癌以及IL-12等多个关键靶点的肿瘤疫苗,为多种癌症的治疗提供了新的选择。
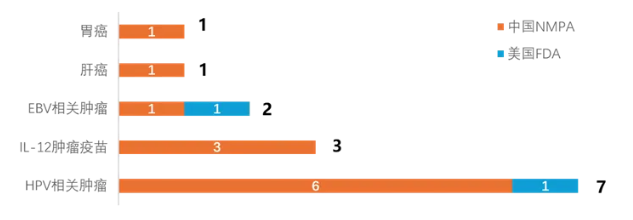
中国mRNA公共抗原肿瘤疫苗在NMPA及FDA的IND申报统计
04 mRNA个性化肿瘤疫苗已进入多个3期临床试验
2024年,Moderna宣布启动mRNA个性化肿瘤疫苗V940 (mRNA-4157) 的多个2期和3期临床试验,适应症涵盖多个癌种。BioNTech也同样布局多个适应症的2期试验,旨在评估其mRNA个性化肿瘤疫苗Autogene cevumeran (RO7198457 , BNT122)的疗效。

mRNA个性化肿瘤疫苗近期开展的Phase 2/3临床试验
国内目前尚无管线申报IND,但是根据Clinical trials、ChiCTR登记的临床数据统计,目前国内已经有30个临床试验,在近两年数量出现猛增,且涵盖多种适应症,包括胃癌、胰腺癌、非小细胞肺癌等晚期实体肿瘤。
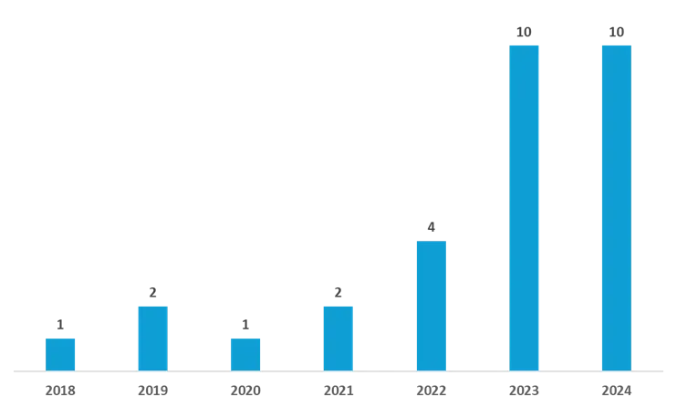
国内mRNA个性化肿瘤疫苗临床登记趋势(Clinical trials & ChiCTR)
相关阅读推荐
三、mRNA 2.0 时代 – 蛋白替代、基因编辑以及in vivo CAR
mRNA 1.0时代,新冠疫苗的成功极大的推动了mRNA技术的发展并迈入2.0时代,其应用范围从传统的疫苗开发拓展到蛋白替代疗法、基因编辑以及in vivo CAR-T等多个前沿领域,并在2024年取得惊人的发展。
01 mRNA蛋白替代疗法开启罕见病治疗新纪元
mRNA蛋白替代疗法是将编码特定蛋白质的mRNA注射到患者体内,使其在细胞内翻译成功能性蛋白质,从而弥补因基因缺陷导致的蛋白质缺失或功能异常。这种疗法为罕见病的治疗带来了新的希望,尤其是那些传统治疗方法难以奏效的疾病。
根据Clinical trials数据,全球约有35个蛋白替代疗法管线,涵盖多种罕见病以及心血管等慢性疾病的治疗,但整体发展尚在Ⅰ期或者Ⅰ/Ⅱ期较早期的阶段。
2024年4月,Moderna公司开发的mRNA蛋白替代疗法mRNA-3927的首个临床试验结果在《Nature》杂志发表。mRNA-3927 用于常染色体隐性遗传儿科代谢疾病丙酸血症,中期分析显示mRNA-3927表现出良好的安全性和耐受性,接受治疗的患者发病风险降低70%。
02 非病毒载体的体内基因编辑药物取得突破
非病毒载体基因编辑药物采用纳米颗粒技术,将基因编辑工具CRISPR-Cas系统直接递送至目标细胞,不仅提高了递送的安全性,还降低了免疫反应的风险。
Intellia的NTLA-2001是FDA首个批准进入临床3期的非病毒载体体内基因编辑疗法,基于 CRISPR/Cas9 技术,通过LNP递送系统靶向肝脏中的 TTR 基因,旨在治疗转甲状腺素蛋白淀粉样变性(ATTR)。2024年6月,Intellia 公布了 NTLA-2001 的最新临床数据。三名患者在接受最低剂量治疗后,进一步接受了55 mg 的重复给药,结果显示血清 TTR 蛋白水平中位数减少了90%,且耐受性良好。
2024年7月和8月,锐正基因针对ATTR的产品ART001分别获得NMPA和FDA的IND审批,成为全球唯一获得中美两国临床许可的同类产品。12月,锐正基因公布IIT病人48周随访结果,结果显示安全性良好,高剂量所有受试者外周TTR蛋白下降幅度均超过90%。
这些卓越的临床表现极大地推动了基于LNP载体的体内基因编辑药物的发展,并显著增强了行业对该技术的信心。
03 in vivo CAR-T取得初步进展
相比于ex vivo CAR-T,基于mRNA / LNP载体的in vivo CAR-T疗法省去了体外的复杂步骤,直接在体内生成CAR-T细胞,可应用于血液瘤、实体瘤、免疫疾病以及遗传疾病等的治疗。In vivo CAR-T降低了生产成本和周期,使患者能够更快地接受治疗。
2024年11月,Capstan在2024年美国风湿病学会(ACR)会议上展示了其基于抗体偶联LNP的mRNA 体内编码CD20 CAR的最新临床前数据。非灵长类体内实验结果显示,外周血和组织中的B细胞经历了深度耗竭,随后以初始B细胞为主的B细胞群体显著回升。这一成果标志着体内CAR-T治疗领域迈出了重要一步,为攻克免疫系统相关疾病带来了新的希望。此外,Capstan的管线预计将于2025年中进入临床试验阶段。
目前,全球范围内in vivo CAR-T疗法的研发正在加速推进。根据公开信息,国内已有超过14家企业布局mRNA/LNP in vivo CAR-T疗法。随着技术的不断成熟和更多临床试验的开展,in vivo CAR-T疗法有望突破现有CAR-T疗法的局限性,为肿瘤、自身免疫性疾病等的治疗提供更高效、更经济的解决方案,进一步推动细胞治疗领域的发展。
四、健新原力RNA卓越中心
健新原力RNA卓越中心致力于为客户提供从质粒到mRNA再到LNP的全流程端到端服务,拥有卓越的技术实力和丰富的项目经验,在mRNA预防性疫苗、mRNA肿瘤疫苗、mRNA蛋白替代等创新药物的项目中取得了显著成就,成功交付多个临床项目,展现了在mRNA全链条创新技术生产服务上的强大实力。
健新原力已于2024年底通过了欧盟QP审计,获得全国首个mRNA药物全流程生产QP符合性声明。标志着健新原力已建立了一套符合国际化标准组织及欧盟GMP标准的质量管理体系,为国际化客户项目以及国内客户出海项目的申报和GMP生产提供了坚实的保障。
相关阅读推荐
参考文献
1.https://www.cnbctv18.com/world/russia-claims-breakthrough-in-cancer-treatment-with-mrna-vaccine-free-for-patients-by-2025-19526110.htm
2.https://www.england.nhs.uk/cancer/nhs-cancer-vaccine-launch-pad/
3.Koeberl, D., Schulze, A., Sondheimer, N. et al. Interim analyses of a first-in-human phase 1/2 mRNA trial for propionic acidaemia. Nature 628, 872–877 (2024). https://doi.org/10.1038/s41586-024-07266-7
4.https://www.prnasia.com/story/471107-1.shtml
5.https://synapse.patsnap.com/blog/capstan-therapeutics-presents-preclinical-findings-on-car-t-candidate-cptx2309
中文 


健新原力
Topping 